Sau đây là bài viết được Kiến thức THPT biên soạn, tổng hợp đầy đủ các lý thuyết este cùng với những bài tập ứng dụng, nhằm mang lại cái nhìn sâu sắc cho bạn đọc.
Bài viết được chia thành hai phần chính: tóm tắt lý thuyết este với thông tin toàn diện từ cấu tạo, phân loại đến danh pháp và tính chất vật lý của este; và phần bài tập, bao gồm những ví dụ cơ bản giúp người đọc củng cố và hiểu rõ hơn về chủ đề này. Hãy cùng tham khảo bài viết để hiểu sâu hơn về este.
Tóm tắt lý thuyết Este lớp 12

Cấu tạo, phân loại
Cấu tạo
Khi nhóm hydroxyl (-OH) trong nhóm cacboxyl của axit cacboxylic được thay thế bằng nhóm oxyalkyl (-OR), ta sẽ tạo thành este.
Este được cấu tạo dựa trên công thức đơn giản như sau:
Trong công thức của este, R và R’ đại diện cho các gốc hiđrocacbon có thể là no, không no hoặc thơm, trừ những este phát sinh từ axit fomic.
Este được xem là một dạng dẫn xuất của axit cacboxylic.
Dưới đây là công thức cấu tạo của một số dẫn xuất khác của axit cacboxylic:
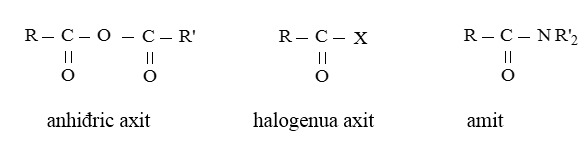
Phân loại
Este no, đơn chức:
Este no, đơn chức có công thức phân tử được biểu thị như CmH2mO2 hoặc CnH2n+1COOCn’H2n’+1, trong đó m tối thiểu là 2 và m bằng tổng của n và n’ cộng thêm 1; n không nhỏ hơn 0 và n’ tối thiểu là 1.
Este không no, đơn chức:
- Este không no, đơn chức, mạch hở có một nối đôi: CmH2m-2O2.
- Este được hình thành từ axit không no và ancol no có công thức: CnH2n-1COOCn’H2n’+1, với n tối thiểu là 2 và n’ ít nhất là 1; m không nhỏ hơn 4.
- Este sinh từ axit no và ancol không no có dạng: CnH2n+1COOCn’H2n’-1, với n từ 0 trở lên, n’ tối thiểu là 2 và m không nhỏ hơn 3 (trong trường hợp n bằng 0, công thức là HCOOCn’H2n’+1).
Este đa chức:
- Este hình thành từ axit đơn chức và rượu đa chức có dạng: (RCOO)mR’, trong đó nếu R’ là glycerol, este có công thức là lipit (RCOO)3C3H5 với R là gốc axit béo.
- Este được tạo bởi axit đa chức và rượu đơn chức có công thức: R(COOR’)n, với n từ 2 trở lên.
- Este sinh từ axit đa chức R(COOH)n và rượu đa chức R’(OH)m có dạng Rm(COO)nmR’n. Nếu m bằng n, este tạo thành có dạng vòng: R(COO)nR’.
Danh pháp
Tên của este được đặt theo công thức: Tên gốc hiđrocacbon R’ + tên anion của axit tương ứng, kết thúc bằng đuôi “at”.
- Dưới đây là một số ví dụ về tên gốc axit phổ biến:
- Axit Fomic (HCOOH) tạo ra anion Fomat (HCOO-).
- Axit Axetic (CH3COOH) tạo ra anion Axetat (CH3COO-).
- Axit Acrylic (CH2=CHCOOH) tạo ra anion Acrylat (CH2=CHCOO-).
- Axit Benzoic (C6H5COOH) tạo ra anion Benzoat (C6H5COO-).
- Các gốc R’ thường gặp bao gồm:
- CH3-: Metyl; C2H5-: Etyl; CH2=CH-: Vinyl
Ví dụ:
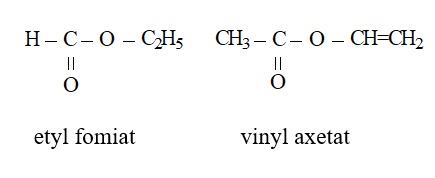
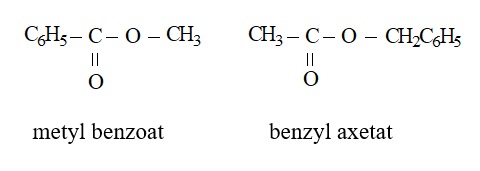
Khi este được tạo từ ancol đơn chức R’OH:
Tên của este được đặt theo quy tắc: Tên gốc hiđrocacbon R’ cộng với tên gốc axit, trong đó đuôi “ic” của axit được thay thế bằng “at”.
Ví dụ:
- CH3COOC2H5 được gọi là etyl axetat.
- CH2=CH-COO-CH3 được gọi là metyl acrylat.
Đối với este sinh từ ancol đa chức:
Tên của este bao gồm tên ancol cộng với tên gốc axit.
Ví dụ:
- (CH3COO)2C2H4 được gọi là etylenglicol điaxetat.
Đối với axit đa chức:
Este này thường được gọi theo tên riêng của chúng.
Ví dụ:
- C3H5(COOC17H33)3 được gọi là triolein, khi axit béo là axit oleic (C17H33COOH).
- C3H5(COOC17H35)3 được gọi là tristearin, khi axit béo là axit stearic (C17H35COOH).
>> Xem thêm: Lý thuyết Saccharose hóa học lớp 12
Tính chất vật lý Este
- Trạng thái: Phần lớn este tồn tại ở dạng lỏng. Tuy nhiên, một số este có trọng lượng phân tử cao có thể ở dạng rắn, như mỡ động vật hay sáp ong.
- Nhiệt độ sôi: Các este thường có nhiệt độ sôi thấp và dễ bay hơi do không có khả năng tạo liên kết hiđro giữa các phân tử.
- Tính tan: Chúng ít tan hoặc không tan trong nước bởi vì este không hình thành liên kết hiđro với các phân tử nước.
- Hầu hết các este đều có mùi thơm nổi bật:
- Isoamyl axetat (CH3COOCH2CH2(CH3)2): mang mùi thơm của chuối.
- Etyl isovalerat ((CH3)2CHCH2COOC2H5): mùi táo.
- Etyl butirat (CH3CH2CH2COOC4H9): mùi thơm của dứa.
- Geranyl axetat (CH3COOC10H17): mùi hoa hồng.
- Benzyl propionat (CH3CH2COO-CH2C6H5): mùi hoa nhài.
Tính chất hóa học Este
Phản ứng ở nhóm chức
Phản ứng thủy phân:
Este có thể bị thủy phân trong cả môi trường axit và kiềm. Khi thủy phân este trong môi trường axit, phản ứng này diễn ra theo chiều ngược lại so với phản ứng este hóa:
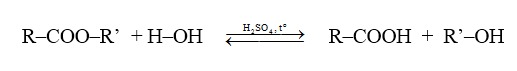
Ví dụ
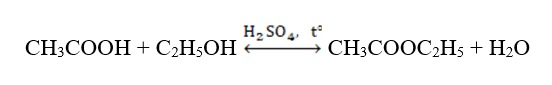
Phản ứng thủy phân este trong môi trường kiềm là phản ứng không thuận nghịch, thường được biết đến với tên gọi là phản ứng xà phòng hóa.
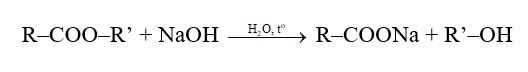
Ví dụ:
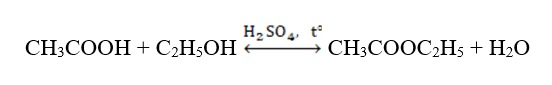
Lưu ý: Khi este dưới dạng lipit (chất béo) được xà phòng hóa, sản phẩm thu được bao gồm glixerol C3H5(OH)3 và xà phòng.

Một số phản ứng thủy phân đặc biệt của este:
Dựa vào các sản phẩm thu được từ phản ứng thủy phân este, chúng ta có thể phỏng đoán được cấu trúc của este ban đầu.
Sau đây là một số trường hợp thủy phân đặc biệt của este (không chứa halogen) thường được nghiên cứu trong các bài toán định lượng:
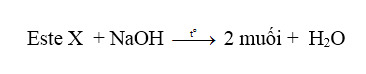
⇒ X là este của phenol, với công thức hóa học là C6H5OOC–R.
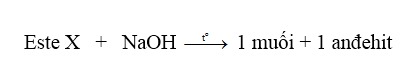
⇒ X là este đơn chức với công thức cấu tạo là R–COO–CH=CH–R’.
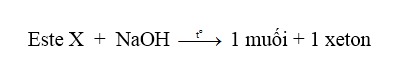
⇒ X là este đơn chức với công thức phân tử R’–COO–C(R)=C(R”)R’’’.
Ví dụ: CH3–COO–C(CH3)=CH2 sẽ tạo thành axeton khi được thủy phân.
⇒ X là este-axit, có công thức cấu tạo là HOOC–R–COOR’.
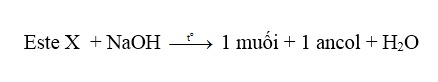
⇒ X là hiđroxi-este với công thức phân tử RCOOCH(OH)–R’.
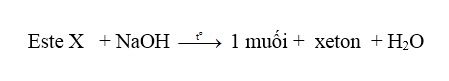
X hiđroxi – este, có công thức là RCOOC(R)(OH)–R’
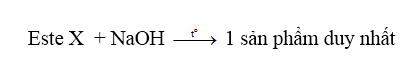
Hoặc “khối lượng chất rắn = khối lượng este + khối lượng NaOH” hoặc “khối lượng sản phẩm = khối lượng este + khối lượng NaOH”
⇒ X là este vòng, được hình thành từ hiđroxi axit, chẳng hạn như:
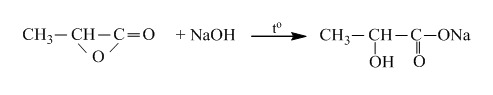
Phản ứng khử
Este được khử bởi liti nhôm hiđrua (LiAlH4), trong quá trình này, nhóm RCO– (còn được gọi là nhóm axyl) chuyển hóa thành ancol bậc một:
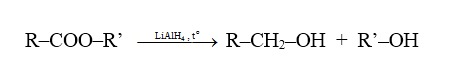
Phản ứng ở gốc hiđrocacbon
Este có khả năng tham gia vào nhiều loại phản ứng hóa học như phản ứng thế, cộng, tách, và trùng hợp. Tuy nhiên, chúng ta sẽ chỉ tập trung xem xét các phản ứng cộng và trùng hợp trong phạm vi bài viết này.
Phản ứng cộng vào gốc không no của este: Gốc hiđrocacbon không no trong este có thể tham gia các phản ứng cộng với H2, Br2, Cl2,… tương tự như các hiđrocacbon không no. Ví dụ:
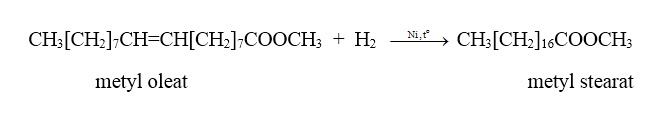
Phản ứng trùng hợp: Các este đơn giản chứa liên kết đôi C=C có thể tham gia vào phản ứng trùng hợp tương tự như các anken.
Điều chế – ứng dụng
Điều chế
Phản ứng giữa axit và rượu:
- Khi axit đơn chức tác dụng với rượu đơn chức:
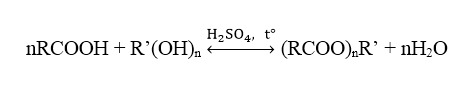
Ví dụ:
Khi axit đơn chức phản ứng với rượu đa chức:
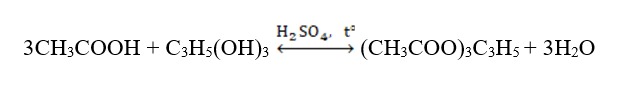
Khi axit đa chức tác dụng với rượu đơn chức:
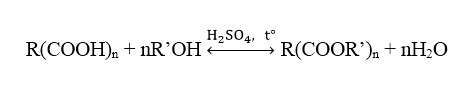
Ví dụ:
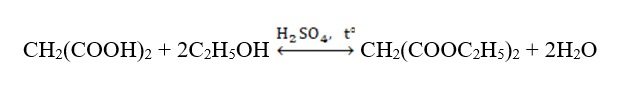
Phản ứng giữa anhiđric axit và rượu
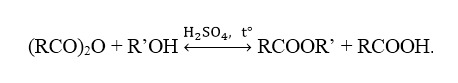
ví dụ:

Ứng dụng
Este được biết đến với khả năng hòa tan tốt các chất hữu cơ, kể cả các hợp chất phân tử lớn, do đó chúng thường được sử dụng làm dung môi trong nhiều ứng dụng, chẳng hạn như butyl và amyl axetat được dùng để pha chế sơn tổng hợp.
Các polyme như poli (metyl acrylat) và poli (metyl metacrylat) được dùng để sản xuất thủy tinh hữu cơ, trong khi poli (vinyl axetat) được ứng dụng trong việc sản xuất các loại nhựa, hoặc có thể thủy phân thành poli (vinyl ancol) để làm keo dính. Một số este của axit phtalic còn được dùng làm chất hóa dẻo và trong sản xuất dược phẩm.
Ngoài ra, một số este có mùi thơm giống hương hoa quả được ứng dụng rộng rãi trong ngành công nghiệp thực phẩm, ví dụ như trong sản xuất bánh kẹo, nước giải khát, và cả mỹ phẩm như xà phòng hay nước hoa.
Nhận biết este
- Este của axit fomic có thể thực hiện phản ứng tráng gương.
- Các este của ancol khi không bền và bị thủy phân sẽ tạo ra anđehit, chất này cũng có khả năng tráng gương.
- Este không no có thể làm mất màu dung dịch brom, cho thấy phản ứng cộng đã xảy ra.
- Khi este của glixerol hoặc các chất béo bị thủy phân, sản phẩm tạo thành có khả năng hòa tan Cu(OH)2.





 111+ hình ảnh cung song ngư nữ anime đẹp nhất full HD
111+ hình ảnh cung song ngư nữ anime đẹp nhất full HD


 Giới thiệu
Giới thiệu Chính sách bảo mật
Chính sách bảo mật Câu hỏi thường gặp
Câu hỏi thường gặp Liên hệ
Liên hệ Kiến thức lớp 10
Kiến thức lớp 10 Cẩm nang học tập
Cẩm nang học tập